ϲѶ��2015��߿����⡪�����ۻ�ѧ���¿α����� 28�� ���� 15�� ��2��2015-07-08 11:27:00���Ķ� �� ��������()����Ͷ��
|
ϲѶ��2015��߿������������ۻ�ѧ���¿α������� 28�� ���� 15�� ��2�� 2015��߿������������ۻ�ѧ���¿α������� http://www.ks5u.com/down/2015-6/29/1798197.shtml �������⣺�Ϻ��к����2015�������ѧ����ĩ��ѧ������ز��Ի�ѧ���� http://www.ks5u.com/down/2015-1/21/1621873.shtml
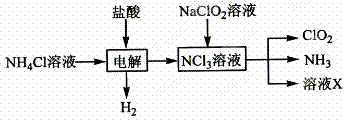
���߿����⡿ 28.(15 �֣�����������ClO2������ɫ������ˮ�����壩�Ǹ�Ч�����������������ش��������}����1����ҵ�Ͽ���KC1O3��Na2SO3��H2SO4�������Ƶ�ClO2���÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ �� ��2��ʵ������NH4Cl�����ᡢNaClO2(�������ƣ�Ϊԭ����ͨ�����¹����Ʊ�ClO2��
����ҺX�д������ڵ���������__________�� ����ȥClO2�е�NH3��ѡ�õ��Լ��� (����)�� a��ˮ b����ʯ�� C��Ũ���� d������ʳ��ˮ ��3������ͼװ�����Բⶨ�������ClO2�ĺ�����
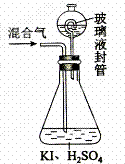
�����ڲ���Һ��װ���м���ˮ��ʹҺ��û������Һ�����Ĺܿ��� ������һ�����Ļ������ͨ����ƿ�����գ� ����������Һ��װ���е�ˮ������ƿ�У� ������0.1000 mol��L-1���������Ʊ���Һ�ζ���ƿ�е���Һ ��I2+2S2O32-��2I��+S4O62-)��ָʾ����ʾ�յ�ʱ����ȥ20.00 mL�� ����������Һ���ڴ˹����У� ����ƿ��ClO2��⻯�ط�Ӧ�����ӷ���ʽΪ �� �ڲ���Һ��װ���������� �� ��V�м����ָʾ��ͨ��Ϊ ���ζ����յ�������� �� ����û������ClO2������Ϊ g�� ��4����ClO2������������ˮ�Ậ��һ�����������������Ҫ��ȥ����������������������������˵���_______������)�� a������ b���⻯�� c������ d���������� ���𰸡�(1) 2��1 ��2����NH4Cl��2HCl ��3����2ClO2��10I����8H����2Cl����5I2��4H2O �����ղ���Ķ����������壨�������ݳ��� �۵�����Һ����Һ����ɫ��Ϊ��ɫ���Ұ��������Һ��ɫ���ٸı� ��0.02700 ��4��d ���������⡿ ���Ϻ��к����2015�������ѧ����ĩ��ѧ������ز��ԡ������12�֣�ʯ����������к��н϶�����⣬��ζ�������ۺ����û��������о����ȵ㡣���������գ� ��1��ʵ���������շ������Ʊ��������壬ԭ�Ͽ�ѡ��__________��ѡ���ţ��� A. ϡ��������ͭ B. ϡ������������ C. ϡ��������п D. Ũ���������� ��Ҫ�õ�һƿ���﴿�������⣬�����շ������⣬��Ӧѡ�õ�װ��������____�����ţ���
��3��һ�ֻ�����ķ�����Ϊ����˹��������Ҫ�������Ƚ�����H2S����ΪSO2������ʣ��H2S���á��������к�67.2 m3 H2S��Ϊ��ֻ�������Ҫ���Ŀ���_____m3���������O2���������Ϊ0.20���� ��4����ҵ�ϳ�������-��ⷨ��������Ҫ���̷������� ��һ������FeCl3��Һ����H2S���˹�������ҺpH_____�����������С�����䡱���� �ڶ��������˺����Һ���е�⣬������Ӧ�����ӷ���ʽΪ��2Fe2++ 2H+ ��5���������һ�ִ������л�����ķ������û�ѧ����ʽ��ʾ����_________________ ���𰸡���1��B��1�֣� �ڢݢޣ���ڢݢۣ���1�֣� ��2���л�ɫ��ĩ������ƿ������СҺ�Σ�2�֣��� ��ʪ���Ʒ����ֽ����ƿ�У���ֽ��ɫ����1�֣������������𰸣� ��3��168��2�֣��� ��4����С��1�֣���FeCl3��Һ��ѭ�����ã�1�֣���4FeCl2 + O2 + 4HCl �� 4FeCl3+ 2H2O��2�֣� ��5��H2S �� H2+ S��H2S + Cl2 �� 2HCl + S��2H2S + O2 �� 2S + 2H2O�ȣ�1�֣��������ɣ��Ƽ������ѣ���http://www.ks5u.com/News/2015-7/111483��
|
��������
������������2024-2025ѧ���һ��ѧ����ĩ����
������������2024-2025ѧ���һ��ѧ����ĩ����
ɽ��ʡ�����в���ѧУ2025-2026ѧ���һ��ѧ��11�������������
ɽ��ʡ�����в���ѧУ2025-2026ѧ���һ��ѧ��11�������������
��������У����2026�������ѧ��12����������
��������
- ����ʡ��У����2025-2026ѧ�������ѧ��1���¿�����
- ����������2026�������ѧ�ڵ�һ����Ӧ�Բ���
- �ӱ�ʡ�����һ����У����2026�������ѧ��1����������
- ����ʡ����Э��У2025-2026ѧ�������ѧ����ĩ����
- ɽ��ʡ������2025-2026ѧ�������ѧ��ĩ����
- ����ʡ��Ȫ��2026�������ѧ����ĩ����
- ����ʡ��˳����У2026�������ѧ����ĩ����
- ɽ��ʡ��������2025-2026ѧ��߶���ѧ��11�����п���

�������
- ϲѶ��2019��߿���Դ���߿�����Ѻ�п���5468��
- ϲѶ��2019��߿����⡪������������ȫ������ ��34�⣨1�� ������50��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(2)
- ϲѶ��2019��߿����⡪�������������������� ��18�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��19�� ������30��
- ϲѶ��2019��߿����⡪������������ȫ������ ��14�� ������18��
- ϲѶ��2019��߿����⡪������������������ ��3�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(1)
�Ƽ�����
- ����ʡ�¸߿���ѧ��������2026�������ѧ��12���������⣨������ʮУ���ˣ����£�
- ��KS5U�������Ĵ�ʡ�ɶ���������ѧ2025-2026ѧ�������ѧ�����п���
- ������ʡ����������ո�����У2025-2026ѧ���һ��ѧ��11�����п���
- �����к�����2025-2026ѧ�������ѧ�����п��ԣ��£�
- ����ʡ÷�ӿ��е�����ѧ2025-2026ѧ�������ѧ��10�����п���
- �㽭ʡ������2025-2026ѧ�������ѧ��9�»�������-
- ����ʡA10����2025-2026ѧ��߶���ѧ��9��ѧ��������⣨�£�
- ��KS5U�������Ĵ�ʡ�ɶ���������ѧ2026�������ѧ�ڿ�ѧ����-