喜讯:2016年高考真题――理科综合化学(全国I卷)第27题 共命中45分 (5)2016-07-06 17:42:00 阅读 次 参与讨论()
|
喜讯:2016年高考真题――理科综合化学(全国I卷)第27题 共命中45分 (5) 【高考真题】 27. (15分)元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4−(绿色)、Cr2O72−(橙红色)、CrO42−(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: (1)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________。 (2)CrO42−和Cr2O72−在溶液中可相互转化。室温下,初始浓度为1.0 mol・L−1的Na2CrO4溶液中c(Cr2O72−)随c(H+)的变化如图所示。
①用离子方程式表示Na2CrO4溶液中的转化反应____________。 ②由图可知,溶液酸性增大,CrO42−的平衡转化率__________(填“增大“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。 ③升高温度,溶液中CrO42−的平衡转化率减小,则该反应的ΔH_________(填“大于”“小于”或“等于”)。 (3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好完全沉淀(浓度等于1.0×10−5 mol・L−1)时,溶液中c(Ag+)为_______ mol・L−1,此时溶液中c(CrO42−)等于__________ mol・L−1。(已知Ag2 CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。 (4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72−还原成Cr3+,反应的离子方程式为______________。 【答案】(1)蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶液写出绿色溶液; (2)①2CrO42-+2H+ (3) 2.0×10-5 ;5×10-3;(4) Cr2O72-+3HSO3- +5H+=2Cr3++3SO42-+4H2O。 【命中试题】 1.【辽宁省部分重点高中协作校2016高三模拟考试理综化学试题 第26 题】 (26)锰及化合物可用于电池、制作坦克的钢甲等材料。 (1)Mn的最高价氧化物的化学式为 ,该氧化物属于 (填“酸性”或“碱性”)氧化物。 (2)工业上常用电解锰酸钾(K2MnO4)溶液的方法制备KMnO4,阴极上的产物为 ___ ,阳极的电极反应式为 ___ 。 (3)以NaBH4和H2O2为原料的燃料电池可用于空军通信卫星电源,该电池的负极材料为石墨,正极材料为MnO2,电解质溶液显碱性。MnO2的作用有两个,分别是作正极材料和 ,负极上的BH4-被氧化为BO2-,该电极的电极反应式为 。 (4)实验室可用软锰矿(主要成分为MnO2)制备KMnO4,其原理如下:高温下,熔融的软锰矿与过量固体KOH反应在不断通入空气的情况下会反应生成K2MnO4(锰酸钾);用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩滤液,得到深紫色的针状KMnO4晶体。 ①用软锰矿制备K2MnO4的化学方程式是 。 ②若用5g软锰矿(MnO2的质量分数为70%)进行上述实验,则KMnO4的理论产量为 g(精确到0.01,不考虑K2MnO4沉淀的循环利用) 【答案】(1)Mn2O7(1分);酸性(1分)(2)H2(2分);MnO42-―e-= MnO4-(2分) (3)作催化剂(2分);BH4-+8OH―+8e-=BO2-+6H2O(2分) (4)①2MnO2+4KOH+O2=2K2MnO4+2H2O(2分); ②4.24(2分)。 2.【福建省厦门市2016届高三下学期第一次教学质量检测理科综合化学试题 第27题】 /down/2016-4/24/2117640.shtml (27)磷化氢( PH3)是一种剧毒气体,是最常用的高效熏蒸杀虫剂,也是一种电子工业原料。 (1)在密闭粮仓放置的磷化铝(AlP)片剂,遇水蒸气放出PH3气体,该反应的化学方程式为 。 (2)利用反应PH3+3HgCl2= P(HgCl)3 +3HCl,可准确测定微量的PH3。 ①HgCl2溶液几乎不导电,说明HgCl2属于____(填“共价”或“离子”)化合物。 ②通过测定溶液____变化,可测定一定体积空气中PH3的浓度。 (3)PH3的一种工业制法涉及的物质转化关系如下图所示:
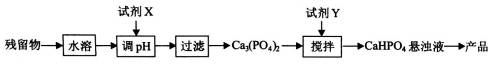
①亚磷酸属于____元酸。 ②当反应I生成的n(NaH2PO2):n(Na2HPO3) =3:1时,参加反应的n(P4):n(NaOH)= -。 (4)一种用于处理PH3废气的吸收剂成分为次氯酸钙80%、锯木屑(疏松剂)15%、活性炭2.5%、滑石粉(防结块)2.5%。 ①次氯酸钙将PH3氧化为H3PO4的化学方程式为____。 ②空气中的水蒸气可加快PH3的氧化过程,其原因可能是____。 (5)从(4)中的吸收残留物中回收磷酸氢钙(CaHPO4)的方法如下:
①试剂x为 (填化学式)。 ②已知25℃时,H3PO4的Kal=7.5×10-3、Ka2=6.3×10-8、Ka3 =4.4×10-13。加入Y时,应控制悬浊液pH 7(填“>”、“=”或“<”),通过计算说明理由 。 【答案】(1)AlP+3H2O====Al(OH)3+PH3。 (2)①共价;②溶液pH或电导率。 (3)①二;② 3:10。 (4)①PH3+2Ca(ClO)2===H3PO4+2CaCl2。②次氯酸钙与水蒸气接触,水解得到氧化性更强的次氯酸。 (5)①>; ②HPO42-的电离常数:Ka(HPO42-)=4.4×10-13,HPO42-的水解常数Kh(HPO42-)=Kw/Ka2=1×10-14/6.3×10-8>Ka(HPO42-),HPO42-的水解程度大于其电离程度,溶液呈碱性,应控制悬浊液pH>7。 3.【山东省临沂市2016届高三下学期教学质量检测(一模)化学试题 第16题】 (16)工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如下:
请回答下列问题: (1)CeCO3F中,Ce元素的化合价为 。 (2)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染。写出稀硫酸、H2O2与CeO2反应的离子方程式: 。 (3)向Ce(BF4)3中加入KCl溶液的目的是 。 (4)溶液中的C(Ce3+)等于1×10-5mol.l-1,可认为Ce3+沉淀完全,此时溶液的pH为 。 (已知KSP[Ce(OH)3]=1×10-20) (5)加热CeCl3 .6H2O和NH4Cl的固体混合物可得到无水CeCl3 ,其中NH4Cl的作用是 。 (6)准确称取0.7500gCeCl3样品置于锥形瓶中,加入适量过硫酸铵溶液将Ce3+氧化为Ce4+,然后用0.1000mol.l-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗25.00ml标准溶液。(已知:Fe2++Ce4+=Ce3++Fe3+) ①该样品中CeCl3的质量分数为 。 ②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,测得该CeCl3样品的质量分数 (填“偏大”、“偏小”或“无影响”) 【答案】(1)+3 (1分)(2)H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑(2分,化学式写错、不配不得分,写化学方程式不得分) (3)避免三价铈以Ce(BF4)3沉淀的形式损失或除去BF4-或提高CeCl3的产率 (2分,合理答案均得分)(4)9(2分) (5)NH4Cl固体受热分解产生HCl,抑制CeCl3水解(2分,合理答案均得分) (6)①82.2%或82.17% (2分) ②偏大(2分) |
网友评论
湖北省十堰市郧阳中学2025-2026学年高二下学期开学考试
湖北省十堰市郧阳中学2025-2026学年高二下学期开学考试