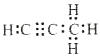ϲѶ��2016��߿����⡪�������ۺϻ�ѧ�������� ��7�� ������42�֣�3��2016-07-06 17:46:00���Ķ� �� ��������()
|
ϲѶ��2016��߿��������������ۺϻ�ѧ�������� ��7�� ������42�֣�3�� ���߿����⡿ 7.��14�֣��±�ΪԪ�����ڱ���һ���֡�
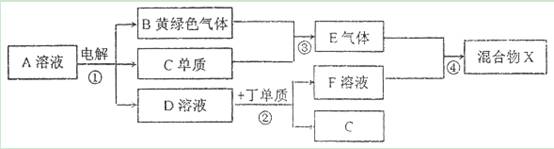
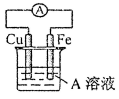
�ش��������� ��1��ZԪ�������ڱ��е�λ��Ϊ__________�� ��2������Ԫ��ԭ�Ӱ뾶������(лԪ�ط���)__________�� ��3��������ʵ��˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����__________�� a��Y������H2S��Һ��Ӧ����Һ����� b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ� c��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ� ��4��X��Z��Ԫ�صĵ��ʷ�Ӧ����1molX����ۻ�����ָ������£�����687kJ����֪�û�������ۡ��е�ֱ�Ϊ-69���58�棬д���÷�Ӧ���Ȼ�ѧ����ʽ__________�� ��5��̼��þ�γɵ�1mol������Q��ˮ��Ӧ������2molMg(OH)2��1mol��������������̼��������Ϊ9:1�����ĵ���ʽΪ__________��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪ__________�� ��6��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ�����������ɱ�������������ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L2.2mol/LNaOH��Һ��1molO2������������ķ���ʽ�����ʵ����ֱ�Ϊ__________����������ͭ���ʵ���Ϊ__________�� ���𰸡���1��������������A�� ��2��Si ��3��ac ��4��Si(s)+2Cl2(g)=SiCl4(l) ��H=-687kJ/mol ��5�� ��6��NO 0.9mol��NO2 1.3mol��2mol ���������⡿ 1.������к�����2016�������ѧ���ܸ�ϰ��������(һ)�����ۺ��Ծ� ��7�� �� ��7)�мס��ҡ��������������ֶ�����Ԫ�أ�ԭ���������������䳣�����ϼ�����Ϊ+1��-2��+1��+3��-1�������γɵ����ʼ��ת����ϵ����ͼ��ʾ���������ö��Ե缫��⣨�������ӽ���Ĥ��1L l mol/L��A��Һ��
�밴Ҫ��ش��������⣺ ��1����Ԫ�����Ԫ��ͬ���壬�ȱ�ԭ�Ӷ�2�����Ӳ㣬��ԭ������Ϊ_____________���Ʋ���ͬ�����±��������ʷֱ���ˮ��Ӧ���ҳ̶ȵ�������_________________________________________�� ��2���ס��ҡ��찴ԭ�������1��1��1�γɵĻ�����Y����Ư���ԣ������ʽΪ___________�� ��3����ͼת����ϵ�в�����������ԭ��Ӧ���У����ţ�____________�� ��4����ͨ��ͼ��·Ƭ�̺����ձ��еμ�һ���Լ����ɼ������缫����ʴ���˷�Ӧ�����ӷ���ʽΪ______��
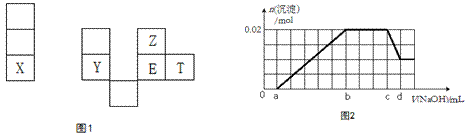
��5������Ӧ�ٵ��һ��ʱ�����D��ҺpH=12�������£�����������ȫ�ݳ���ȡ������Ĥ����Һ��ֻ��ȣ�������Һ����仯������ʱ��ת�Ƶ�����ĿԼΪ________����Ӧ�ڵ����ӷ���ʽΪ___________�� ��6������ͼ�и�����Ӧ��Ϊǡ����ȫת����������X�к��е����ʣ���ˮ�⣩��_________________�� ���𰸡�(14��)(1) 37��2�֣�������ͬ����Ԫ�صĽ�������˵���������Ӷ���ǿ���Ʋ⼺������ˮ��Ӧ�ϱ������ң�1�֣��������֣�(2) ��4��3Fe2++2[Fe(CN)6]3- =Fe3[Fe(CN)6]2��(2��)�� ��5�� 2.������кӶ���2016�����һģ���������ۺϻ�ѧ�Ծ� ��7�⡿ ��7��X��Y��Z��E��T��Ϊ������Ԫ�أ������ڱ��е����λ����ͼ1��X�Ƕ�������ԭ�Ӱ뾶����Ԫ�أ� X��Y��ͬһ���ڣ�Y�dz����İ뵼����ϣ� E������������Ӧˮ������ǿ��ˮ�ԡ�
�����жϳ���Ԫ�ػش����⣺ ��1�� T��Ԫ�����ڱ��е�λ�� �� ��2�� �⼸��Ԫ�ص��⻯���У�ˮ��Һ������ǿ���� (�ѧʽ)�� YZ2 ���۵� EZ2 ���۵�(����ڻ����)�� ��3��E2T2 �ĵ���ʽ �� ��4����ҵ���Ʊ�����X�Ļ�ѧ��Ӧ����ʽ �� ��5����֪1mol����Y������Z2��ȼ�գ��ָ������£��ų�989.2 kJ ������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ���� ��6��ij��Һ�п��ܺ�������������(������ˮ���������H����OH��)��H����NH4����K����Mg2����Al3������ȡ100mL����Һ��εμ�NaOH��Һ����ó��������ʵ�����NaOH��Һ�������ϵ����ͼ2��ʾ�� ����ʵ���У�NaOH��Һ����b��c�ι����з��������ӷ�Ӧ����ʽΪ ��NaOH��Һ��Ũ��Ϊ mol��L��1 (����ĸc��d��ʾ���� ��ԭ��Һ�к��е�Mg2����Al3����H���������ʵ���֮��n��Mg2������n��Al3������n��H����Ϊ �� ���𰸡���1���������ڵ���A�壻(2)HCl�����ڣ���3�� ��4��2NaCl ��� =2Na+Cl2���� ��5��Si(s)��O2(g)�TSiO2(s)����H����989.2 kJ��mol�D1 ��6����NH4+ + OH-= NH3��H2O��10/(d-c) mol��L��1 ���� 1��1��1 . 3. ������кӶ���2016������ڶ���ģ�⿼�Ի�ѧ���� ��7�⡿/down/2016-5/3/2129553.shtml ��7���±��������ֶ�����Ԫ�ص������Ϣ��
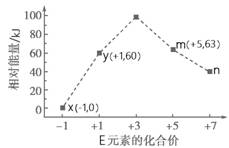
�밴Ҫ��ش��������⣺ ��1��DԪ�غ�������Ų� �� ��2��A��B��Ԫ���γɵĺ��зǼ��Լ��Ļ�����Ľṹʽ ��A��B��Ԫ���γɵľ�����ͬ�������������У��ѧʽ����______________��_____________�� ��3��C��A�γɵ�ijһ�������ܺ�C��B�γɵ���һ��ɫ������(�����ֻ����������ԭ�Ӹ����Ƚ�Ϊ1��2)һ������������Ƽ������߷�����Ӧ���������ʣ�д��������ѧ��Ӧ����ʽ�� �� (4)һ�������£���ˮ��Һ��1 mol E����EO(x��1,2,3,4)������(kJ)��Դ�С����ͼ��ʾ��n�� (�����ӷ���)�����ӷ�Ӧy��x��m���Ȼ�ѧ����ʽΪ ��
��5��Na2DB3ˮ��Һ�и�����Ũ�ȵĴ�С˳���� �������ӷ��ţ��� ���𰸡���14�֣� ��1�� ��3��2N2H4+N2O4==3N2+4H2O ��2�֣���4��ClO4����1�֣� �� 3ClO��(aq) = 2Cl��(aq) +ClO3��(aq) ��H����117 kJ��mol-1��2�֣� ��5��Na+>SO32->OH->HSO3->H+��2�֣�
�Ƽ������ѣ���http://www.ks5u.com/News/2016-7/127542��
|
��������
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����2026�������ѧ��1��һģ���⣨�£�
��������

�������
- ϲѶ��2019��߿���Դ���߿�����Ѻ�п���5468��
- ϲѶ��2019��߿����⡪������������ȫ������ ��34�⣨1�� ������50��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(2)
- ϲѶ��2019��߿����⡪�������������������� ��18�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��19�� ������30��
- ϲѶ��2019��߿����⡪������������ȫ������ ��14�� ������18��
- ϲѶ��2019��߿����⡪������������������ ��3�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(1)
�Ƽ�����
- ������У����2026�������ѧ�ڡ�3+3+3���߿����������������һ��
- ����ʡ�¸߿���ѧ��������2026�������ѧ��12���������⣨������ʮУ���ˣ����£�
- ��KS5U�������Ĵ�ʡ�ɶ���������ѧ2025-2026ѧ�������ѧ�����п���
- ������ʡ����������ո�����У2025-2026ѧ���һ��ѧ��11�����п���
- �����к�����2025-2026ѧ�������ѧ�����п��ԣ��£�
- ����ʡ÷�ӿ��е�����ѧ2025-2026ѧ�������ѧ��10�����п���
- �㽭ʡ������2025-2026ѧ�������ѧ��9�»�������-
- ����ʡA10����2025-2026ѧ��߶���ѧ��9��ѧ��������⣨�£�