ϲѶ��2017��߿����⡪����ѧ�����Ͼ�����13�� ������28��2017-06-28 13:54:00���Ķ� �� ��������()
|
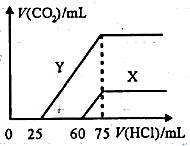
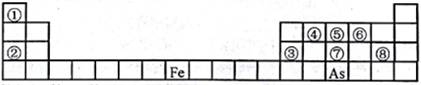
ϲѶ��2017��߿�����������ѧ�����Ͼ��� �����ƶ�������28�� ���߿����⡿2017��߿������������ۣ����Ͼ�����13�� 13��X��Y��L��MΪ�˵�������������ǰ20������Ԫ�أ�X2����������壬Y��L��M����Ԫ�ص���������Ϊ5�ı������ش��������⣺ ��1��X��L��ɵ��������ĵ���ʽΪ�� ���� ��2��X��M��ɵ�����Ϊ�� ������������������������������������ʿ���ΪҰ�����Ӧ��ȼ�ϣ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ�� ���� ��3��Y�����ڱ��е�λ���ǡ� �����京����Ļ�ѧʽΪ�� ���� ��4��L��M�γɵĻ�������L�Ļ��ϼ��ǡ� ���� ���𰸡���1��X��L��ɵ��������ΪPH3������ʽ���ư�����Ϊ ��2��X��M��ɵ�����ΪCaH2��Ϊ���ӻ��������ˮ��Ӧ��������������ʽΪCaH2+2H2O�TCa��OH��2+2H2���� �ʴ�Ϊ�����ӣ�CaH2+2H2O�TCa��OH��2+2H2���� ��3��YΪBԪ�أ�λ�����ڱ��ڶ����ڢ�A�壬������ΪH3BO3���ʴ�Ϊ���ڶ����ڢ�A�壻H3BO3�� ��4��L��M�γɵĻ�����Ca3P2��Ca�Ļ��ϼ�Ϊ+2�ۣ�PΪ��3�ۣ��ʴ�Ϊ����3�� ����������һ������к�ƽ��2017������������������飨��ģ����ѧ���� Word�溬�� 7. ( 14�֣�A��B��C��D��E��F�Ƿ������������ڵ�����Ԫ�أ���ԭ��������������A��Dͬ���壬B���⻯��ˮ��Һ�ʼ��ԣ�C��Eͬ���壬�γɵĻ�����EC2���γ��������Ҫ����֮һ���뻯ѧ����ش��������⣺ ��1��F��Ԫ�����ڱ��е�λ��Ϊ_______________�� ��2�������£�Һ̬��B2A4����̬��BC2���߷�����Ӧ���������ʣ�16g B2A4������Ӧ����akJ���÷�Ӧ���Ȼ�ѧ����ʽΪ_______________�� ��3��D2E��Һ�ڿ����г��ڷ��÷�����Ӧ��������֮һΪH��H��������ƵĽṹ�ͻ�ѧ�������ƣ�����Һ�Ի�ɫ��H�ĵ���ʽΪ_______��д���ڿ����г��ڷ�������H�Ļ�ѧ��Ӧ����ʽΪ��_____________��H����Һ��ϡ���ᷴӦ����������Ϊ_____________�� ��4����ѧ�ҷ���һ�ֻ�ѧʽΪA4B4�����ӻ����һ��������1mol A4B4���ڵ��������������Ӹ�1mol�������������ʱ�ĵ��뷽��ʽΪ____________�� ��5����30mLijŨ����A��B��C��D������Ԫ���γ�һԪǿ����Һͨ��CO2��������ҺM����CO2ͨ�����IJ�ͬ����ҺM�����Ҳ��ͬ������M����μ���0.1mol/L���ᣬ����������V(CO2)�������������V[HCl(aq)]�Ĺ�ϵ������ͼʾ�������������CO2���ܽ⣩�� ������Y����M�е�����Ϊ________��ԭNaOH��Һ�����ʵ���Ũ��Ϊ_______��������X��Y��֪������ʵ��ͨ���CO2�������Ϊ_________�� ���𰸡���1���������ڵڢ�A�壨2�֣��� ��2��2N2H4(l)+2NO2(g)=3N2(g)+4H2O(l) ��H=-4akJ/mol��2�֣��� ��3�� ��4��NH4N3 ��5��NaHCO3��Na2CO3��1�֣���0.25mol/L��1�֣���3:10��1�֣��� �����������������кӱ���2017������ܸ�ϰ������� ��һ�������ۺ����� Word�溬�� /down/2017-4/22/2660226.shtml 7.��14�֣���ͼ��Ԫ�����ڱ���һ���֡� I.�û�ѧ����ش��������⣺ ��1���ڡ��ޡ�������Ӱ뾶�ɴ�С��˳��Ϊ_________�������ӷ��ű�ʾ���� ��2���ܡ��ߡ������ۺ������������ǿ������˳����_______�����û�ѧʽ��ʾ�� ��3��As��ԭ�ӽṹʾ��ͼΪ_______�����⻯��Ļ�ѧʽΪ_______�� ��4��Y�ɢڢޢ�����Ԫ����ɣ�����ˮ��Һ�������г�������������As����Y��ˮ��Һ��Ӧ��������As����ۺ����ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ_________��������1mol��ԭ��ʱ������ת����______mol�� ��.A��B��C��D��E��X���������ڱ�����Ԫ����ɵij������ʻ����֪A��B��C��D��E��X������ͼ��ʾת����ϵ������������ͷ�Ӧ������ȥ������������AΪ����ɫ���壬BΪǿ�ᣬXΪ�����������ʡ� ��5��A��ˮ��Ӧ�Ļ�ѧ����ʽΪ_______________�� ��6����ҵ�ϳ����Ȼ�ԭ��ұ��X��д���仯ѧ����ʽ___________�� ��7��ij�¶��£�>100������m��X��H2O��Ӧ�ų�QkJ��Q>0����������д���÷�Ӧ���Ȼ�ѧ����ʽ_______________�� ���𰸡���1��Cl->O2->Na+��1�֣� ��2��HClO4>H3PO4>H2CO3��1�֣� ��3�� ��4��NaClO+2As+3H2O=2H3AsO4+NaCl��2�֣�5��2�֣� ��5��3NO2+H2O=2HNO3+NO��2�֣� ��6��Fe2O3+3CO ��7��3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) ��1=-168Q/mkJ/mol��2�֣� �Ƽ������ѣ���http://www.ks5u.com/News/2017-6/146026��
|
��������
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����2026�������ѧ��1��һģ���⣨�£�
��������

�������
- ϲѶ��2019��߿���Դ���߿�����Ѻ�п���5468��
- ϲѶ��2019��߿����⡪������������ȫ������ ��34�⣨1�� ������50��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(2)
- ϲѶ��2019��߿����⡪�������������������� ��18�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��19�� ������30��
- ϲѶ��2019��߿����⡪������������ȫ������ ��14�� ������18��
- ϲѶ��2019��߿����⡪������������������ ��3�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(1)
�Ƽ�����
- ������У����2026�������ѧ�ڡ�3+3+3���߿����������������һ��
- ����ʡ�¸߿���ѧ��������2026�������ѧ��12���������⣨������ʮУ���ˣ����£�
- ��KS5U�������Ĵ�ʡ�ɶ���������ѧ2025-2026ѧ�������ѧ�����п���
- ������ʡ����������ո�����У2025-2026ѧ���һ��ѧ��11�����п���
- �����к�����2025-2026ѧ�������ѧ�����п��ԣ��£�
- ����ʡ÷�ӿ��е�����ѧ2025-2026ѧ�������ѧ��10�����п���
- �㽭ʡ������2025-2026ѧ�������ѧ��9�»�������-
- ����ʡA10����2025-2026ѧ��߶���ѧ��9��ѧ��������⣨�£�