ϲѶ��2019��߿����⡪�����ۻ�ѧ��ȫ������28�⣨����65�֣���1��2019/7/30 9:55:00���Ķ� �� ��������()
|
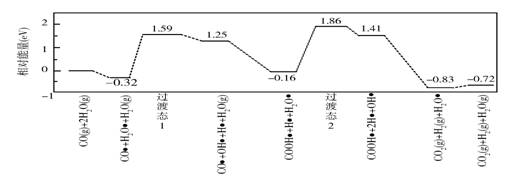
ϲѶ��2019��߿����⡪�������ۺϣ�ȫ������ ���߿����⡿2019��߿����⡪�������ۺϣ�ȫ������ ��28�� https://www.ks5u.com/down/2019-6/9/3700680.shtml 28����14�֣� ˮú���任[CO(g)+H2O(g)=CO2(g)+H2(g)]����Ҫ�Ļ������̣���Ҫ���ںϳɰ��������Լ��ϳ����ӹ��ȹ�ҵ�����С��ش��������⣺ ��1��Shibata����������ʵ�飺��ʹ��H2������ͨ������721 ���µĹ���������CoO(s)�������ܲ��ֱ���ԭΪ������(Co)��ƽ���������H2�����ʵ�������Ϊ0.0250�� ����ͬһ�¶�����CO��ԭCoO(s)��ƽ���������CO�����ʵ�������Ϊ0.0192�� ��������ʵ�����жϣ���ԭCoO(s)ΪCo(s)��������CO_________H2����������������С�������� ��2��721 ��ʱ�����ܱ������н������ʵ�����CO(g)��H2O(g)��ϣ������ʵ��Ĵ������з�Ӧ����ƽ��ʱ��ϵ��H2�����ʵ�������Ϊ_________�����ţ��� A����0.25 B��0.25 C��0.25~0.50 D��0.50 E����0.50 ��3���ҹ�ѧ�߽��ʵ��������ģ�������о����ڽ����������ˮú���任�ķ�Ӧ���̣���ͼ��ʾ�����������ڽ���������ϵ�������
��֪ˮú���任����H________0������������������������С����������������������ݣ���ܣ�E��=_________eV��д���ò���Ļ�ѧ����ʽ_______________________�� ��4��Shoichi�о���467 ����489 ��ʱˮú���任��CO��H2��ѹ��ʱ��仯��ϵ������ͼ��ʾ��������Ϊ��������ʵ���ʼʱ��ϵ�е�PH2O��PCO��ȡ�PCO2��PH2��ȡ�
��������a�ķ�Ӧ��30~90 min�ڵ�ƽ������ ���𰸡� ��1������ ��2��C ��3��С�� 2.02 COOH*+H*+H2O*===COOH*+2H*+OH*����H2O*=== H*+OH*�� ��4��0.0047 b c a d ����������1��14�� ����ʡ������������2019�������ģ���ԣ�ʮһ����ѧ�Ծ� Word�溬��https://www.ks5u.com/down/2019-7/12/3734172.shtml 20. (14��)�����仯�������������������й㷺��Ӧ�á� (1)����������������(MnFe2O4)�������Ȼ�ѧѭ���ֽ���������ԭ�����£� ��MnFe2O4(s)===MnFe2O(4��x)(s)��O2(g)����H1 ��MnFe2O(4��x)(s)��xH2O(g)===MnFe2O4(s)��xH2(g)����H2
����H3����H1����H2�Ĺ�ϵΪ��H3��________�� (2)����������Ҫ�Ĵ���������������з�Ӧ�Ƶã�Fe(s)��5CO���Fe(CO)5(g)����H<0����1 L�����ܱ������м����������ۺ�0.5 mol CO����T1��T2��ͬ�¶��½��з�Ӧ�����c(CO)���¶ȡ�ʱ��Ĺ�ϵ��ͼ1��ʾ��ͼ1
��T1________(����>������<��)T2�� ��T2�¶�����������Ӧ��ƽ�ⳣ��K��________(�����Ҫ�����λ)�� (3)�������(K2FeO4)�����dz�Ϊ����ɫ��ѧ����ˮ������������������������������²��ȶ��� ����ҵ����KClO��Fe(NO3)3��Һ��Ӧ�Ƶ�K2FeO4����Ӧ�����ӷ���ʽΪ________________________________________���Ʊ�K2FeO4ʱ��KClO������Һ��Fe(NO3)3������Һ��ϵIJ���Ϊ________________________�� ����֪K2FeO4��ˮ���������Ԫ���γɵ����ֲ�������pH�Ĺ�ϵ��ͼ2��ʾ��
ͼ2ͼ3 ��pH��6����Һ�м���KOH��Һ��������Ӧ�����ӷ���ʽΪ____________________________________�� (4) ��ⷨ���Ƶ�K2FeO4��װ����ͼ3��ʾ�������ĵ缫��ӦʽΪ______________________________________�� ���𰸡� (1) (2��) (2) ��>(2��) ��8��103(2��) (3) ��3ClO����2Fe3����10OH��===2FeO��3Cl����5H2O(2��) �ڽ����£���Fe(NO3)3������Һ�����μӵ�KClO������Һ��(2��) ��HFeO��OH��===FeO��H2O(2��) (5) Fe��6e����8OH��===FeO��4H2O(2��) (6)
����������2��12�� ����ʡ������������2019�������ģ���ԣ�ʮһ����ѧ�Ծ�+Word�溬��https://www.ks5u.com/down/2019-7/12/3734172.shtml 21. (12��) A. [���ʽṹ������] ������ͭ�ķ�Ӧ֮һΪ2CuFeS2��O2Cu2S��2FeS��SO2�� (1) Cu����̬��������Ų�ʽΪ________________��
(2) Cu��Zn�ĵڶ������ܣ�I2(Cu)________(����>����<����������)I2(Zn)�� (3) SO2������Sԭ�ӵĹ���ӻ�����Ϊ________�����ӵĿռ乹��Ϊ________����SO2��Ϊ�ȵ�����ķ�����________(дһ��)�� (4) [Cu(CH3CN)4]���Ƿdz��ȶ���������ӣ���������������������֮��Ϊ________�� (5) Fe2����Fe3������CN����ϣ���ṹ��ͼ��ʾ�������ӿ��γ��������Σ��ü��εĻ�ѧʽΪ________�� ���𰸡� A. [���ʽṹ������] (1) [Ar]3d10 (2) > (3) sp2�� V�Ρ�O3 (4) 5��2 (5) KFeFe(CN)6 ����������3��12�� ����ʡ������������2019�������ģ���ԣ�ʮһ����ѧ�Ծ�+Word�溬��https://www.ks5u.com/down/2019-7/12/3734172.shtml
B. [ʵ�黯ѧ] 8�ǻ����( ����ͼ1��ʾ����������ƿ�м����������͡����������ӡ��ڰ������Ӻ�Ũ���ᡣ
ͼ1ͼ2 ����������Ӧ�Զ����ҽ��С� ����Ϊˮ��������װ�ý���ˮ��������ֱ�����Һ�в���������Ϊֹ�� ����������ƿ�м���һ����NaOH��Һ�����ٵμӱ���Na2CO3��Һ��pH����7��8�� �����½���ˮ���������������Һ�в����о��������� �������Һ�����ȴ���������һ�����Ƶò�Ʒ�� (1)ͼ1����ȴˮӦ��________(����A������B��)�ڽ��� (2)ͼ2��ˮ��������װ�á���һ��ˮ���������Ŀ����___________________________________�� �������ܳ��ֶ���ʱ��ͼ2�пɹ۲쵽��������_________________________________________�� (3)����װ����������©���������ƿ�IJ��ֲ��˹�������ԭ����________________________________�� (4)���������ƿ���Դ����Ӧ���Զ����ҽ��е�ԭ����__________________________________�� (5)�������м���ı���Na2CO3��Һ���ܹ�����ԭ����__________________________________�� ���𰸡� B. [ʵ�黯ѧ] (1) A(2��) (2) ��δ��Ӧ�ķ�Ӧ�������(2��)����������ˮλ����(2��) (3) ��ֹ��Һ�������ƿ֧�ܶ������ѹϵͳ(2��) (4) ��Ӧ�ų���������(2��) (5) �������Na2CO3��Һ����������ǻ�ҲҪ��Na2CO3��Ӧ��������(2��) ����������4��12�� ����ʡ��Ϫ����ѧ2019�������ģ���Ի�ѧ�Ծ�+Word�溬��https://www.ks5u.com/down/2019-7/11/3731731.shtml 21��������(SO2Cl2)��һ����Ҫ�Ļ����Լ����Ȼ����Ǻϳ�������(SO2Cl2)�ij��÷����� ʵ���Һϳ������ȵ�ʵ��װ������ͼ��ʾ(���ּг�װ��δ����)��
��֪���� SO2(g) + Cl2(g)��SO2Cl2(l) ��H����97.3 kJ/mol�� �� �����ȳ�����Ϊ��ɫҺ�壬�۵�Ϊ��54.1�����е�Ϊ69.1�����ڳ�ʪ���������������� �� 100�����ϻ�ʱ���������ȶ��ֽ⣬���ɶ�������������� �ش��������⣺ (1) װ��A�з�����Ӧ�����ӷ���ʽΪ�� (2) װ��B������Ϊ����ȱ��װ��C��װ��D��SO2��Cl2 �����ܷ�����Ӧ�Ļ�ѧ����ʽΪ�� (3) ����F������Ϊ��E������ˮ�������(����a������b��)�� F������Ϊ�� (4) ��װ��A���ų�����1.12 L(������ɱ�״��)ʱ�����յõ�5.4 g�����������ȣ��������ȵ� ����Ϊ��Ϊ��߱�ʵ���������ȵIJ��ʣ���ʵ���������Ҫע������� ��(�����)�� �� ��ͨ����ˮ����ͨ�� �� �����������ʣ��������˿� �� ��������ƿ���̣����ʵ����� �� ����������ƿ (5) �Ȼ���(ClSO3H)���ȷֽ⣬Ҳ���Ƶ�������2ClSO3H��SO2Cl2 + H2SO4���������ķ����� A���ؽᾧ B������ C������ D����ȡ (6) ���ڴ�ŵ��������ᷢ�ƣ���ԭ�����Ϊ�� ���𰸡� (1) 2MnO4�� + 10Cl�� + 16H+��2Mn2+ + 5Cl2��+ 8H2O�� 1���� (2) ��ȥHCl �� 1�֣� SO2 + Cl2 + 2H2O��2HCl + H2SO4�� 2�֣� (3) ���θ���� �� 1���� a�� 1���� ��ֹ�����е�ˮ�������룻����β����������Ⱦ������ 2�֣� (4) 80% �� 1�֣� �٢ڢ��� 2�֣� (5) (5) C �� 1�֣� (6) �����ȷֽ���������ܽ����������е����䷢���� 1�֣� ����������5��5�� ����ʡ�����е���ʮ����ѧ2019�����5��ģ�⻯ѧ�Ծ�+Word�溬��https://www.ks5u.com/down/2019-7/4/3724424.shtml 23.��5�֣�ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3�����������������ۣ���Һ�� Fe2��Ũ�Ⱥͼ������۵����ʵ���֮��Ĺ�ϵ��ͼ��ʾ����ϡ��Һ��Fe(NO3)3��Cu(NO3)2��HNO3���ʵ���Ũ��֮��Ϊ ����Ӧ���Ⱥ�˳��д���ù��̵����ӷ�Ӧ����ʽ�� ���𰸡�1:1:4 Fe+4H++NO3-= Fe3++NO��+2H2O 2 Fe3++ Fe=3 Fe2+ Cu 2++ Fe=Fe2++Cu
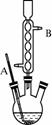
����������6��10�� ����ʡ�����е���ʮ����ѧ2019�����5��ģ�⻯ѧ�Ծ�+Word�溬��https://www.ks5u.com/down/2019-7/4/3724424.shtml 25.��10�֣�FeCl3���ִ���ҵ������Ӧ�ù㷺��ij��ѧ�о���ѧϰС��ģ�ҵ�����Ʊ���ˮFeCl3�����ø���ƷFeCl3��Һ�����ж���H2S�� �������������ϵ�֪����ˮFeCl3�ڿ������׳��⣬����������������������Ʊ���ˮFeCl3��ʵ�鷽����װ��ʾ��ͼ�����ȼ��г�װ����ȥ���������������£�
������װ�õ������ԣ� ��ͨ������Cl2���Ͼ�װ���еĿ����� ���þƾ�������м�·���������Ӧ��ɣ� �ܡ��� ����ϵ��ȴ��ֹͣͨ��Cl2�����ø����H2�Ͼ�Cl2�����ռ����ܷ⡣ ��ش��������⣺ ��1��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ�� ��2�����������Ⱥ����ɵ���״FeCl3�ֽ����ռ��������������ڷ�Ӧ��A�Ҷ�Ҫʹ������FeCl3�����ռ����������������ǡ� ��3�����������У�Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ�У������ţ��� ��4��װ��B����ˮԡ������Ϊ��װ��C������Ϊ��װ��D��FeCl2ȫ����Ӧ����ʧȥ����Cl2�����ö�ʧЧ��д������FeCl2�Ƿ�ʧЧ���Լ����� ��5�������߿��л���β������װ��E��ע���Լ��� ��������ͬѧ��װ��D�еĸ���ƷFeCl3��Һ����H2S���õ��������˺�����ʯīΪ�缫����һ�������µ����Һ�� ��6��FeCl3��H2S��Ӧ�����ӷ���ʽΪ�� ��7���ۺϷ���ʵ������������Ӧ����֪��ʵ�������������ŵ㣺 ��H2S��ԭ��������Ϊ100%������ ���𰸡� (1)2Fe+3Cl2 (2)�ڳ�����FeCl3�����·����� (3)�ڢ� (4)��ȴ��ʹFeCl3�����������ռ���Ʒ����� K3[Fe(CN)6)��Һ (5) (6)FeCl3��H2S��Ӧ�����ӷ���ʽΪ 2Fe3++H2S=2Fe2++S��+2H+ (7)FeCl3�õ�ѭ������
�Ƽ������ѣ���https://www.ks5u.com/News/2019-7/176578��
|
��������
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡ��ɳ��´ɽ����ʵ��ѧУ2025-2026ѧ���һ��ѧ��4��ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����������ѧ2025-2026ѧ��߶���ѧ�ڿ�ѧ����
����ʡʮ����2026�������ѧ��1��һģ���⣨�£�
�������

�������
- ϲѶ��2019��߿���Դ���߿�����Ѻ�п���5468��
- ϲѶ��2019��߿����⡪������������ȫ������ ��34�⣨1�� ������50��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(2)
- ϲѶ��2019��߿����⡪�������������������� ��18�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��19�� ������30��
- ϲѶ��2019��߿����⡪������������ȫ������ ��14�� ������18��
- ϲѶ��2019��߿����⡪������������������ ��3�� ������18��
- ϲѶ��2019��߿����⡪������������ȫ������ ��33�⣨2�� ������50��(1)
�Ƽ�����
- ������У����2026�������ѧ�ڡ�3+3+3���߿����������������һ��
- ����ʡ�¸߿���ѧ��������2026�������ѧ��12���������⣨������ʮУ���ˣ����£�
- ��KS5U�������Ĵ�ʡ�ɶ���������ѧ2025-2026ѧ�������ѧ�����п���
- ������ʡ����������ո�����У2025-2026ѧ���һ��ѧ��11�����п���
- �����к�����2025-2026ѧ�������ѧ�����п��ԣ��£�
- ����ʡ÷�ӿ��е�����ѧ2025-2026ѧ�������ѧ��10�����п���
- �㽭ʡ������2025-2026ѧ�������ѧ��9�»�������-
- ����ʡA10����2025-2026ѧ��߶���ѧ��9��ѧ��������⣨�£�