1.下列物质中含离子键的是( )
a.cl2 b.co2
c.nacl d.ch4
解析:选c。nacl为离子化合物,含有离子键。
2.下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合形成稳定化合物的是( )
a.10与19 b.6与16
c.11与17 d.14与8
解析:选c。根据离子键的形成条件,活泼金属元素与活泼的非金属元素间一般形成离子键,根据原子序数,c项中是na和cl符合题意。
a.形成离子键的阴、阳离子间只存在静电吸引力
b.hf、hcl、hbr、hi的热稳定性和还原性均依次减弱
c.第三周期非金属元素含氧酸的酸性从左到右依次增强
d.元素周期律是元素原子核外电子排布周期性变化的结果
解析:选d。a项,形成离子键的阴、阳离子间既存在静电吸引力,又存在静电排斥力;b项,hf、hcl、hbr、hi的热稳定性依次减弱,还原性依次增强;c项,第三周期非金属元素最高价含氧酸的酸性从左到右依次增强;d项,元素原子核外电子排布的周期性变化导致元素性质的周期性变化,即元素周期律。
4.下列化合物电子式书写正确的是( )
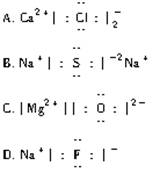
资源难易程度:★★★★★★★★★★★★★★★
高考资源网版权所有 ©2005-2010
未经许可,盗用或转载本站资料者,本站将追究其法律责任!